再鼎医药PARP抑制剂尼拉帕利(Niraparib,商品名“则乐”)获国家药品监督管理局(NMPA)批准上市,用于对含铂化疗完全或部分缓解的复发性上皮性卵巢癌、输卵管癌或原发性腹膜卵巢癌成人患者维持治疗。这是全球首款获批用于所有铂敏感复发卵巢癌患者群体(无论BRCA是否突变)的PARP抑制剂,也是国内获批的第2款PARP抑制剂。
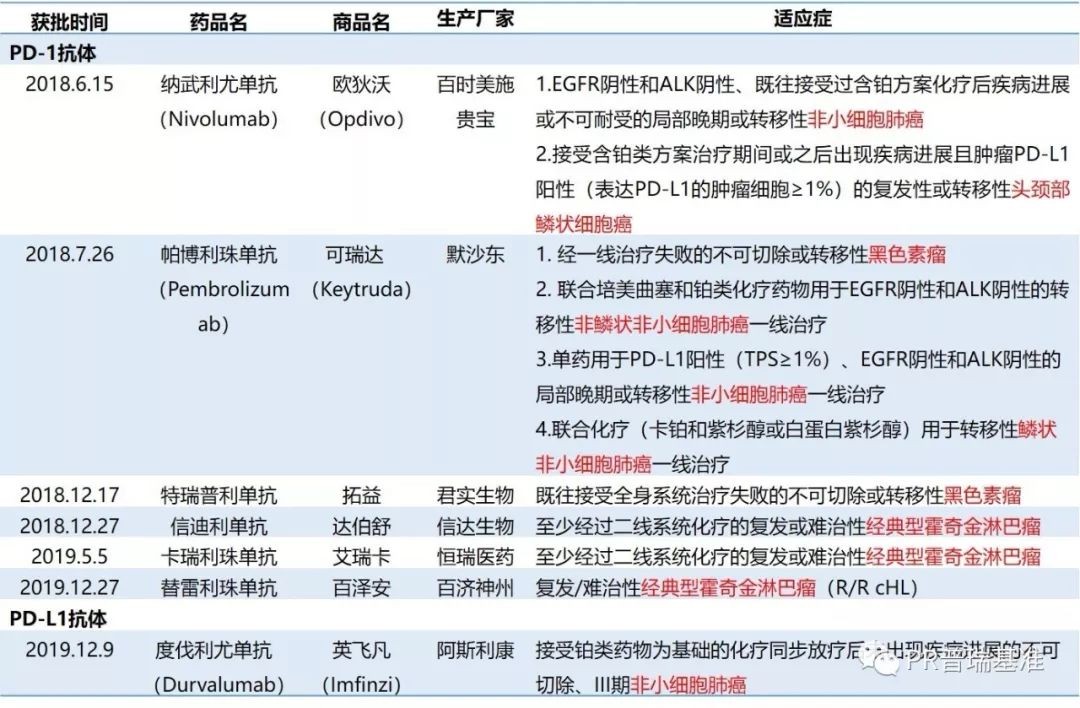
同日,百济神州PD-1抗体替雷利珠单抗(Tislelizumab,BGB-A317)获NMPA批准上市,治疗复发/难治性经典型霍奇金淋巴瘤(R/R cHL)患者。至此,国内已有7款PD-1/PD-L1抑制剂获批上市。
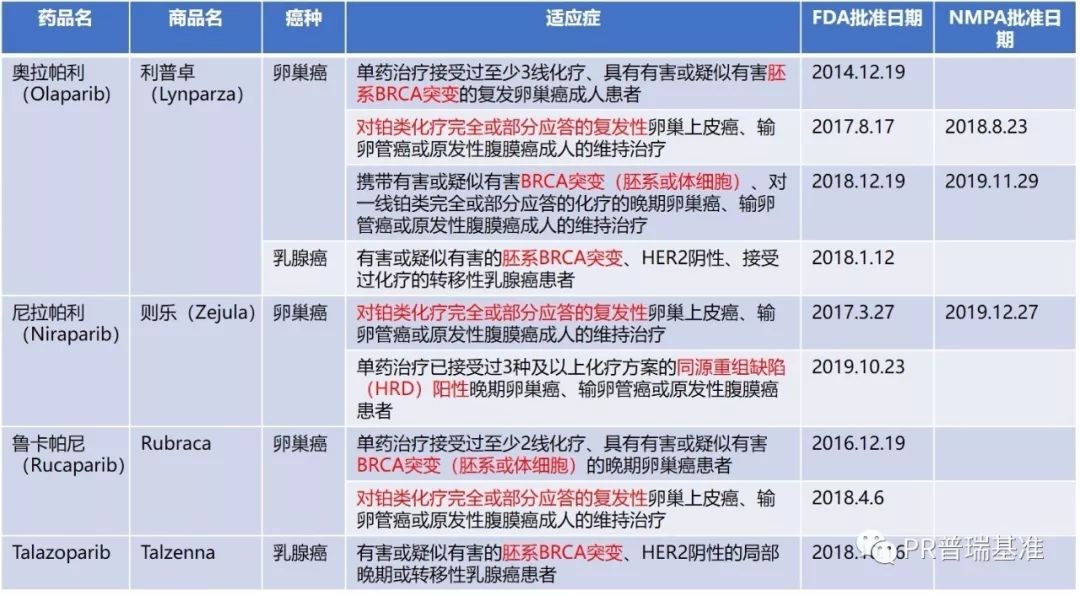
尼拉帕利创首个超越BRCA的PARPi
尼拉帕利用于铂敏感复发卵巢癌维持治疗的获批是基于III期的NOVA研究。研究招募了553位含铂治疗有效的复发性卵巢癌、输卵管癌或原发性腹膜癌患者,按照2:1的比例接受尼拉帕利或者安慰剂维持治疗。
PARPi和PD-1接连获批,普瑞基准助力精准用药
随着尼拉帕利等PARP抑制剂的适应症不断拓展,卵巢癌、乳腺癌、前列腺癌、胰腺癌、胃癌、小细胞肺癌、非小细胞肺癌等癌症患者都迎来了更多希望。尤其随着同源重组修复(HRR)基因突变、HRD Score等标志物的评估出现,获益人群已从BRCA突变人群扩展至HRD阳性人群。此外,国产PD-1的不断涌现也为中国患者带来了更多长期生存的希望。PD-L1蛋白表达、TMB、MSI-H/dMMR作为免疫治疗标志物也写入了多种实体瘤的NCCN现行指南。
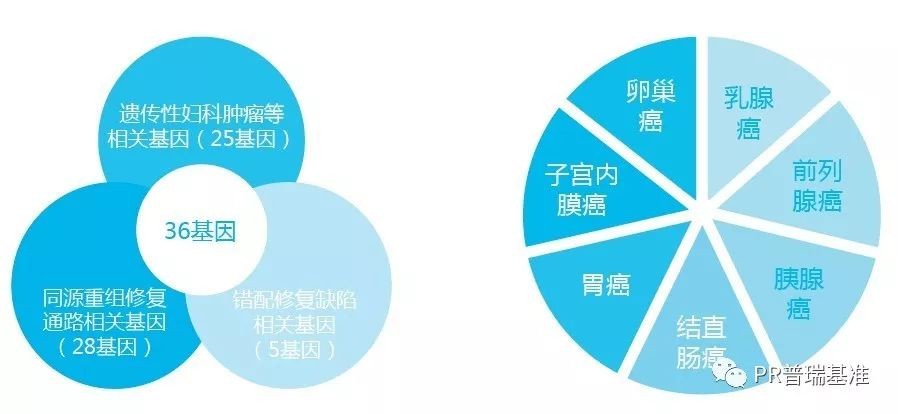
普瑞基准科技推出的昂可迪系列产品,通过对包含HRD和dMMR相关基因在内的遗传性妇科肿瘤相关36个基因进行胚系和体系变异检测,指导肿瘤患者对PARP抑制剂、PD-1/PD-L1抑制剂的适用性,并准确评估遗传性妇科肿瘤及其它肿瘤的遗传风险。在此基础上,普瑞基准联合北京协和医院共同发起了全国首个卵巢癌HRD大型研究,建立中国卵巢癌患者的HRD Score模型,相比BRCA检测可将卵巢癌PARP抑制剂获益人群扩大3倍。
在2018年中国医疗器械行业协会主办的精准医学精标准——“NGS BRCA校准计划”中,普瑞基准满分通过了BRCA 突变注释考核,以及胚系BRCA1/2突变检出、分析、解读的测评,充分体现了我们在变异检测和解读方面的实力。此外,普瑞基准已连续满分通过多项国家卫生健康委临床检验中心(NCCL)室间质评,为我们的临床检测产品和生物信息分析服务提供了质量保障。